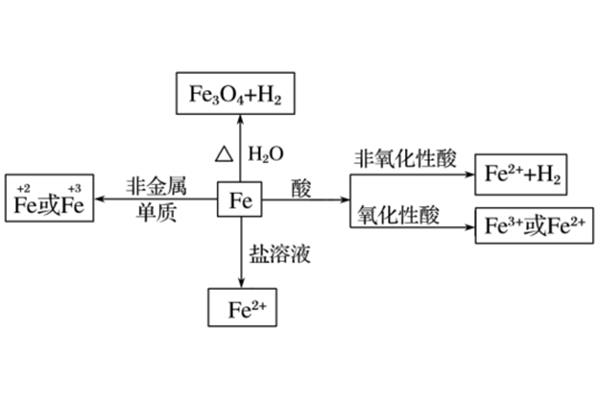
初中化学方程式及实验现象汇总建议多背背
N5。初中化学方程式和实验现象|||化学方程式也叫化学反应方程式,是用化学式表示化学反应的公式,化学方程式反映了客观事实,以下是编译好的初中化学方程式,欢迎阅读参考。以下分解反应代替其他物质的通用名及其对应的化学式来代替反应化学方程式,应用初中化学超完备方程和实验现象总结真的很有用,建议打印出来背一背,各种实验现象和方程都很清楚。如有需要,请收藏,完整的电子版,后台私密,

浓硝酸分解反应方程式is:4 HNO 32 hoo 2↑4 NO2↑。由于浓硝酸不稳定,在光照下会分解二氧化氮,使溶液变黄,所以浓硝酸常放在棕色试剂瓶中,置于阴凉处,而稀硝酸相对稳定。在冷硝酸中加入铁或铝,如果没有明显现象,则为浓硝酸,如果铁或铝表面出现气泡,则为稀硝酸。浓硝酸的性质如下:1 .浓硝酸是一种强酸,具有酸的共性。

110℃分解反应:NHNO → NHHNO (no氧化还原反应)在185℃ ~ 200℃,分解反应如下:氧化产物与还原产物的比例为1: 1 (n为5,加热到300℃左右时,2nhno→ 2no4ho的氧化产物与还原产物的摩尔比为3: 5 (n分别从5和3变为0)。硝酸铵(NH₄NO₃)是一种铵盐,无色无味透明晶体或白色晶体,易溶于水,易吸潮结块,溶解时吸收大量热量。
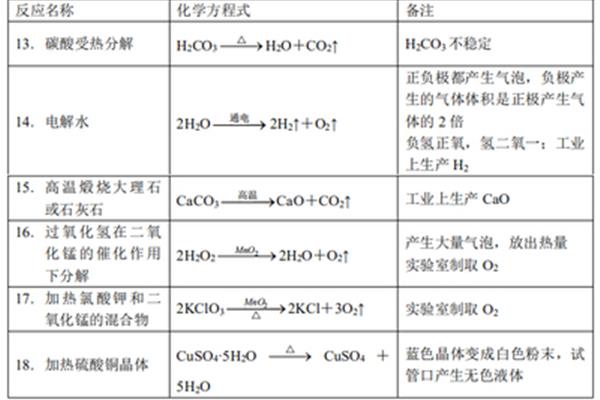
它是一种氧化剂,用于化肥和化学原料。扩展资料:浓硝酸不稳定,遇光或受热会分解释放出二氧化氮,二氧化氮溶于硝酸中,从而使外观呈淡黄色。但是稀硝酸相对稳定。反应方程式:4无光照4no₂↑o₂↑2h₂o4hno₃△4no₂↑o₂↑2h₂o o↑2 hopure硝酸铵在室温下稳定,对冲击、碰撞或摩擦不敏感。

分解反应:(如果是初三,应该主要记得前四个)1。水通电→氢氧2、二氧化锰过氧化氢→氧水3、高锰酸钾加热→二氧化锰钾氧4、氯酸钾锰2、加热→氯化钾氧5、氧化汞加热→汞氧6、碳酸钙高温→氧化钙二氧化碳7、碳酸氢钠加热→

(1)与单质的分解反应:水通电后反应生成氢气和氧气。这个反应的化学方程式是:2H2O带电。2h2 = O2 =。(2)与单质的化学反应:碳和氧被点燃时,生成二氧化碳。这个反应的化学方程式是:C O2被点燃。(3)仅与化合物的分解反应:当加热碱式碳酸铜时。水和二元碳。该反应的化学方程式为:Cu2 (OH) 2co3△ .2cuoh2oCO2 ↑。所以答案是:(1)2H2O带电。2 H2↑O2↑;

分解反应:氯酸钾和二氧化锰共加热(实验室自制O2):2 kclo 3(MnO 2△2 KCl 3 o 2 =加热的高锰酸钾:2kmno4 △ k2mn4mno2o2 =加热的碱式碳酸铜:Cu2(OH)。2CO3△2CuO H2O CO2↑电解水:2H2O带电2h2 O2 ↑碳酸不稳定组分H2CO3H2O CO2↑高温煅烧石灰石:CaCO3高温CaCO3硫酸铜晶体受热失去结晶水:cuso 4·5H2O△cuso 4·5H2O氢氧化铜受热变成Cu(OH)2△CuO·H2O。

摘要:1。直流电作用下水的分解:2H2O2 ↑ H2 ↑ O2 ↑现象:(1)电极上产生气泡。H2: O2 = 2: 1正极产生的气体能使带火星的木条重燃。负极产生的气体可以在空气中燃烧,产生淡蓝色的火焰。2.加热碱式碳酸铜:Cu2(OH)2CO32CuO H2O CO2↑现象:绿色粉末变黑,试管内壁生成水滴,澄清的石灰水变浑浊。

n H4 no 2n 22 H2O 2n H4 no 32n 24 H2O 23 NH 2 oh 3n 2 H3 H2 hn3 N2 h 21。加热过氧化锰(加热高锰酸钾)2KMnO4K2MnO2 O2(气体)2。碳酸不稳定,分解H2CO3H2O CO2(气体)3。煅烧石灰石CaCO3CaO CO2(气体14。过氧化氢)催化产氧:2H2O2(MnO2催化)2H2O O2↑15。直流电作用下水的分解:2H2O带电2H2↑ O2↑16。加热碱式碳酸铜:Cu2(OH)。2CO3加热2CuO H2O CO2↑17。加热氯酸钾(加少量二氧化锰):2kcl3o2 ↑ 18。加热高锰酸钾:2KMnO4加热K2MnO4mo2o2 ↑ 19。碳酸不稳定,分解:H2CO3H2O CO2↑20。高温煅烧石灰石:CaCO3高温CaO CO2↑化学反应1)单质与氧气的反应。: 1.镁在氧气中燃烧:2毫克氧气点燃2毫克氧气。铁在氧气中燃烧:3Fe 2O2点燃Fe3O43。铜在氧气中加热:2Cu O2加热2CuO4。铝在空气中。
8、复 分解反应方程式20个![{$DT[sitename]}](/skin/zx123/img/logo.png)