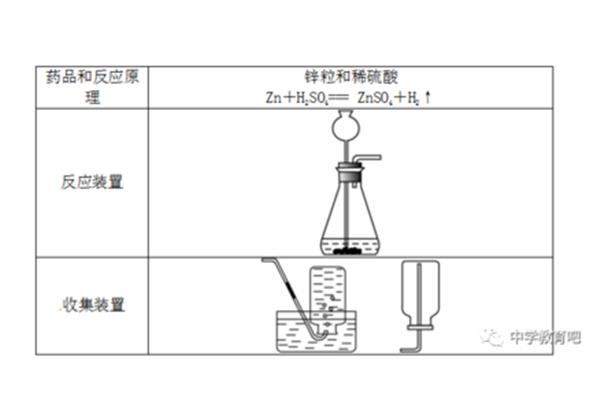
所有能与酸反应的金属酸会和许多金属发生反应吗?
活泼金属与酸反应生成氢气,是置换反应。金属不同,酸不同,化学反应的种类也不同,如较活泼的金属与稀强酸反应会生成盐和氢气,如Zn 2HCl=ZnCl2 H2,这种反应是置换反应,有些金属不与稀酸反应。酸性是由氢离子表现出来的性质,金属活动性顺序表中H前面的金属可与某些酸:盐酸或稀硫酸反应生成氢气,因此就表现出了酸性。

1酸和金属会发生反应;2酸会释放氢离子(H ),金属会往往失去电子,生成相应的阳离子(通常是金属离子),从而形成盐和氢气;3通常可以写成。一、定性分析1、氢前金属和非氧化性酸(如盐酸、稀硫酸等)反应时得到的是H₂。例如Zn H₂SO₄=ZnSO₄ H₂↑。2、氢前金属和氧化性酸(如稀硝酸、浓硫酸。酸和金属氧化物反应生成盐和水,例如:氧化铁和稀硫酸反应:Fe2O33H2SO4==Fe2(SO4)33H2O;氧化铜和稀盐酸反应:CuO2HCl==CuCl2H2O。

锌和稀硫酸反应:Zn H2SO4==ZnSO4 H2↑;镁和稀硫酸反应:Mg H2SO4==MgSO4 H2↑;铝和稀硫酸反应:2Al 3H2SO4==Al2(SO4。这是初中化学知识:活泼性排在H之前的金属都能和酸发生反应,生成盐和H2;具体的有:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb。
镁和稀盐酸反应生成氯化镁和氢气,和稀硫酸反应生成硫酸镁和氢气,反应的化学方程式为:Mg 2HCl═MgCl2 H2↑,Mg H2SO4═MgSO4 H2↑。锌和稀硫酸Zn H2SO4=ZnSO4 H2↑铁和稀硫酸Fe H2SO4=FeSO4 H2↑镁和稀硫酸Mg H2SO4=MgSO4 H2↑铝和稀硫酸2Al 3H2SO4=Al2(SO4。
![{$DT[sitename]}](/skin/zx123/img/logo.png)